Magyar kutatók fényt derítettek a hosszú covid kialakulásában szerepet játszó agyi folyamatokra

Nagy előrelépést tettek magyar kutatók annak megértésében, hogy mitől alakulnak ki a covidbetegséggel járó idegrendszeri tünetek, és miért bizonyulhatnak sok esetben tartósnak. Az innovatív módszereket felhasználó kutatás világszerte sok millió, hosszú coviddal élő embernek adhat reményt, hogy szindrómájukat a jövőben könnyebb lehet majd diagnosztizálni és kezelni.
A COVID-19-ért felelős SARS-CoV-2 vírus 2019 végén bukkant fel a kínai Vuhanban, ahonnan gyorsan globális terjedésnek indult. A három éven át tartó világjárvány az Egészségügyi Világszervezet (WHO) hivatalos statisztikája szerint 765 millió megbetegedést okozott és 6,9 millió áldozatot követelt, de a kórokozó valójában a Föld lakosságának nagy részét legalább egyszer megfertőzte. A vakcinák és a fertőzés több hulláma által kialakított védettségnek hála a járvány 2023-ra véget ért, de ahogy arra a legtöbb szakember számított, a vírus nem tűnt el teljesen, hanem az influenzához hasonlóan endemikussá vált. És nemcsak a vírus maradt velünk, hanem a covidbetegségek utóhatásai is: a WHO becslése szerint a fertőzöttek 6 százalékánál poszt-covid szindróma alakult ki, ami fáradékonysággal, légszomjjal, izomfájdalommal vagy alvászavarral járhat.
„Az egyik nagyon komoly oka a hosszan elnyúló poszt-covidos tüneteknek az lehet, hogy az agyi gyulladást nagyon nehéz rendbe tenni, és ennek központi eleme a mikroglia sejtek funkcióváltozása” – mondta a Qubitnek Dénes Ádám, a HUN-REN Kísérleti Orvostudományi Kutatóintézet (KOKI) Neuroimmunológia Kutatócsoportjának vezetője, amikor március végén irodájában beszélgettünk. Az agykutató kollégáival öt évvel ezelőtt kezdte vizsgálni, hogy milyen gyulladásos folyamatokat indít be az emberi agyban a COVID-19, és hogyan hat az agyi környezethez speciálisan alkalmazkodott, mikrogliáknak nevezett immunsejtek működésére. Ennek eredménye az a tanulmányuk is, ami nemrég jelent meg a világ vezető idegtudományi folyóiratában, a Nature Neuroscience-ben.
Lényegében minden olyan fertőzés, amely immunválaszt okoz és megemeli a keringésben a gyulladásos faktorok szintjét, eléri az idegrendszert, ami e faktorok agyi hatásainak köszönhetően enyhébb esetben fáradékonysághoz vagy étvágytalansághoz vezet. A COVID-19-nél a vizsgálatok 30-60 százalék közé teszik az idegrendszeri tünetek előfordulását, amik a szaglás ideiglenes elvesztésétől a kognitív funkciók és memória romlásával járó „covid-ködön” át egészen súlyos idegrendszeri tünetekig terjednek. „Nagyon kevés olyan esetet tudunk, ahol semmilyen idegrendszeri érintettség nem igazolható” – mondta Dénes, akinek az elmúlt években elért kiemelkedő kutatási eredményeiért a Magyar Tudományos Akadémia Elnöksége tavaly Akadémiai Díjat adományozott.

Azt már a járvány elején sejteni lehetett a tünetek különbözőségéből, mondta a szakember, hogy a COVID-19 különböző agyterületeket érint, és az idegrendszeri érintettség nincs szoros összefüggésben a tüdőt érintő betegség lefolyásának súlyosságával. Voltak, akiknél a megbetegedés miatt elvesztett szaglás és ízérzékelés hetek vagy hónapok után sem állt helyre, és sok poszt-covidos beteg tünetei, például a fáradékonyság, levertség, fejfájás vagy a vegetatív idegrendszer érintettsége miatt kialakuló magas vérnyomás, évek múltán sem oldódtak meg. Ebben Dénesék szerint komoly szerepe lehet annak a nehezen regenerálódó, gyulladásos tünetegyüttesnek, ami a fertőzés során eléri az agyat.
Ahhoz, hogy vizsgálataikat lefolytathassák és kideríthessék, milyen változásokat okoz a központi idegrendszerben – vagyis az agyban és a gerincvelőben – a COVID-19, előbb emberi szövetmintákhoz kellett jutniuk. Dénes szerint ez a járvány kezdeti időszakában jelentős szervezési munkát igényelt. Végül a Korányi Pulmonológiai Intézet biztosította, hogy a szakemberek biztonságos körülmények között elvégezhessék a covidban elhunyt betegek boncolását, miközben más forrásokból nem covidos betegektől származó mintákhoz jutottak, amiket kontrollként használtak. A kutatás során egy új módszertant is kidolgoztak, ami csúcstechnológiás mikroszkópokkal, a különböző agyi sejtek által kifejezett mRNS-t felderítő szekvenálással, fehérjeszintű vizsgálatokkal, valamint mesterséges intelligenciával azonosította a COVID-19 által okozott gyulladást és idegrendszeri károsodást.
Nem okoz tömeges idegsejt fertőzést, de súlyos gyulladást okozhat
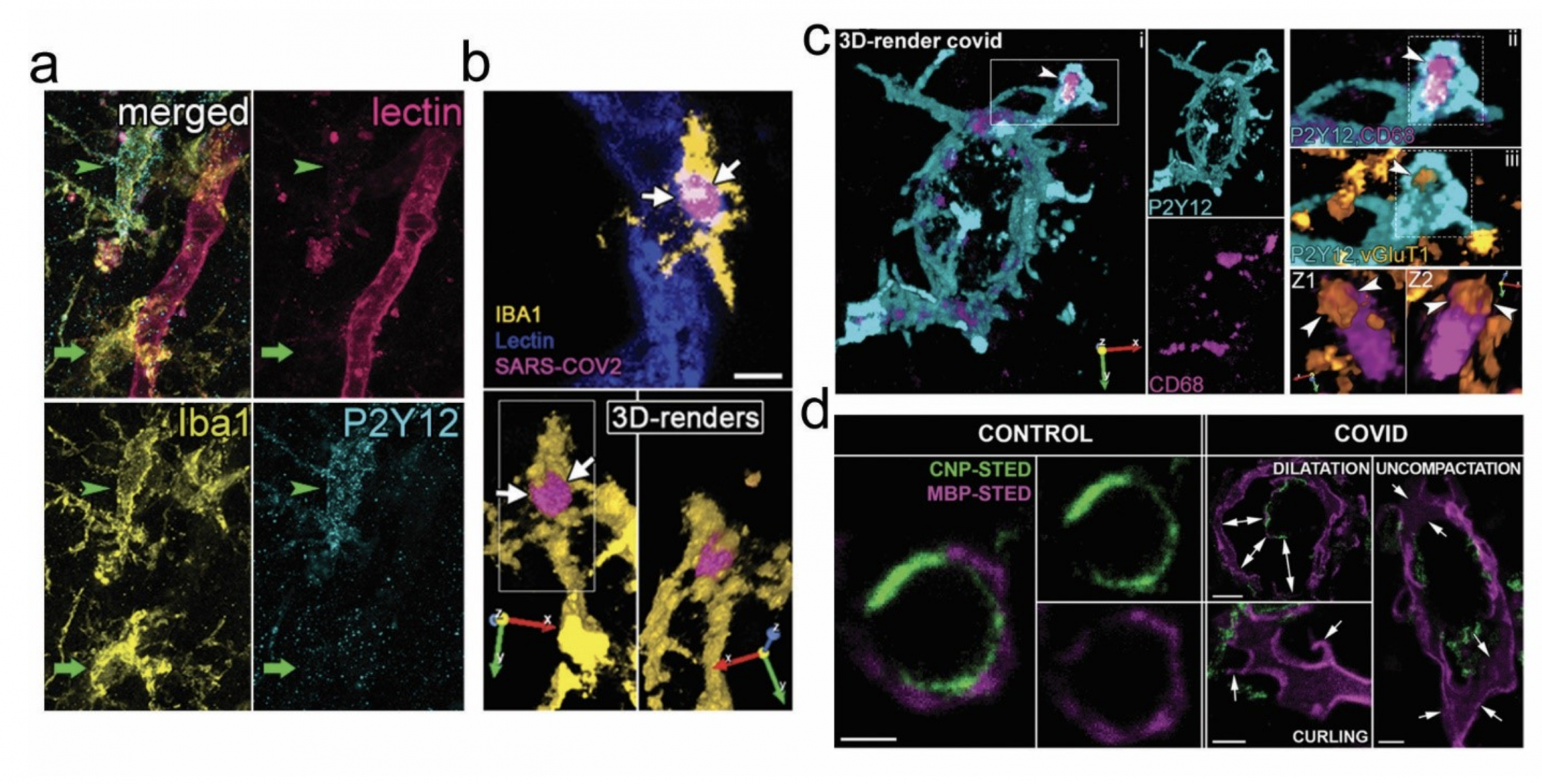
A koronavírusok neurotróp vírusok, vagyis képesek az idegszövetet és az idegsejteket is megfertőzni. A járvány kezdetén így Dénes szerint az tűnt valószínűnek, hogy a SARS-CoV-2 magukat az idegsejteket fertőzi, de aztán érkeztek adatok, amik ennek ellentmondtak. Emiatt a kutatás során külön figyelmet fordítottak arra, hogy meg tudják határozni, a megbetegedés pontosan milyen agyi területeket és sejteket érint. Arra jutottak, hogy a kórokozó nem fertőzi meg nagy számban az idegsejteket vagy a gliasejteket, köztük az immunsejtként funkcionáló mikrogliákat. Ehelyett a vírusfertőzés hatására létrejövő, jelentős gyulladás elsősorban az agy keringését és energiaellátását biztosító agyi erek falában volt kimutatható, ahol vírusfehérjéket is azonosítottak.
Az egyik legfontosabb megfigyelésük az volt, hogy a COVID-19-ben elhunyt betegek agyában a mikroglia sejtek, amiket Dénes kutatócsoportja már régóta vizsgál, a gyulladt agyi erek köré gyűltek. De vajon miért érdemelnek ezek a sejtek kitüntetett figyelmet? A mikrogliák az agyszövet elsődleges immunsejtjei, amiknek több különböző immunsejt funkcióját kell egyszerre ellátnia. A sejtek nemcsak, hogy fontos szerepet játszanak az agyi immunfolyamatokban és a vírusfertőzések elleni védelemben, hanem segítik az idegsejtek és idegi hálózatok megfelelő működését, valamint az agyi keringést is. Régebbi vizsgálataikból és más kutatásokból azt is tudták a szakemberek, hogy súlyos idegrendszeri megbetegedések kialakulásában és súlyosbodásában jelentős szerepet játszanak a szervezetben jelentkező, szisztémás gyulladásos folyamatok, valamint az idegrendszer és az immunrendszer között fennálló kapcsolatok. Ismert volt az is, hogy a keringésben lévő gyulladásos anyagok nagymértékben képesek az agyi mikroglia sejtek működését átalakítani.
A mikrogliák sérülésekre és fertőzésekre érzékeny „szenzorok” és „kapuőrök”, így alapvetően nem meglepő, hogy a COVID-19-es betegek agyszövetében a gyulladt erek köré gyűltek. Az erek falában nemcsak vírusfehérjéket mutattak ki, hanem a vérkeringést az agyi állománytól elválasztó vér-agy gát sérülését is, márpedig ha a vérben keringő fehérjék elkezdenek ellenőrizetlenül bekerülni az agyi állományba, az idegrendszeri működési zavart okoz. Erre a mikrogliák is érzékenyek, és ez lehet az egyik oka annak, hogy az erekhez sereglő sejtek közül sok elhalt. „Azokon a területeken, ahol a mikroglia a legkomolyabb zavart mutatta, ott volt a legsúlyosabb az idegi patológia” – mondta Dénes, ami többek közt az idegsejtek közötti speciális kapcsolatok, a szinapszisok elvesztésében és az idegsejtek axonjait szigetelőkábelként borító mielinhüvely sérülésében nyilvánult meg. Korábbi, képalkotó eljárásokkal poszt-covidos betegekben végzett klinikai vizsgálatok egybevágnak az eredményeikkel, és azt mutatják, hogy a vér-agy gát sérülése összefügghet a mikrogliák működési zavaraival és a betegek idegrendszeri tüneteivel.
Miközben az idegi patológia súlyossága agyterületenként változó volt, a mikroglia sejtek alakja (és ezáltal a működésük) a fertőzés hatására nagyon sok agyterületen megváltozott, ami összefüggést mutatott az erek és idegsejtek sérülésével is. Egy ilyen terület, ahol különösen gyakran figyeltek meg változásokat, az agytörzs volt, ahol a fő légzés- és keringésszabályozó központok vannak. „A mikroglia sejtek, hogyha egyetlen egy gyulladásos stimulust is kapnak, életükben bármikor, az örökre megváltoztatja működésüket” – mondta a kutató, vagyis ha megindul bennük egy gyulladásos folyamat, akkor hetekkel vagy hónapokkal később sem nyugszanak meg. Ezt klinikai adatok is igazolják, és Dénes szerint ez lehet az egyik oka a poszt-covidos tünetek elhúzódásának.
Még szembeötlőbb volt a mikrogliák működési zavara, amikor a sejtek által kifejezett fehérjéket és enzimeket vizsgálták: a gyulladt erekhez sereglett mikrogliák elveszítették kulcsfontosságú receptoraikat, amelyekkel normális esetben az idegi hálózatok, valamint az agyi erek működését segítik. Kísérleteikből az is világossá vált, hogy az immunsejtek működési zavara összefügg azzal, hogy az adott agyszövetből mennyire sok virális RNS-t tudtak kimutatni. Ezután arra keresték a választ, hogy a sejteken belül vajon mi vezet a mikrogliák funkciózavarához. A választ, úgy tűnik, a mitokondriumnak nevezett, kvázi a sejt „erőműveként” szolgáló sejtszervecskék környékén kell keresni, amik ősei a komplex élet kialakulása előtt baktériumok voltak. A mikroglia sejtek működése és aktivitásváltozása Dénes szerint egy nagyon intenzív mitokondriális működést igényel, valamint a mitokondriális funkció megváltozását is. Vizsgálataik a COVID-19 hatására mitokondriális működési zavarra utaló fehérjéket mutattak ki, amely okozhatja a mikroglia sejtek gyulladásos folyamatainak zavarát, illetve pusztulásukat is.
Felderítették a COVID-19-re jellemző gyulladási mintázatot
A kutatók azt is fel szerették volna tárni, hogy a COVID-19 pontosan milyen molekuláris szintű változásokhoz vezet az agyban és a gerincvelőben. Ehhez feltérképezték, hogy miként változtak meg az agy-gerincvelői folyadékban (liquor), valamint egyes agyterületeken jelen lévő fehérjék, amiből következtetni lehet arra, hogy a fertőzés hatására milyen fehérjék fejeződnek ki. Dénes szerint két nagy cél van, amiért ezeket a fehérjemintázatokat érdemes megismerni: egyrészt új terápiás lehetőségek kidolgozása, másrészt új biomarkerek azonosítása, amelyek egyértelműen jeleznék a COVID-19 idegrendszeri károsodásban betöltött szerepét. Utóbbi lehetővé tenné, hogy egy poszt-covidos beteg állapotát a gerincvelői folyadékból diagnosztizálják, és hatékonyabb kezelési javaslatokat tudjanak nekik adni.
Ezeknek az úgynevezett proteomikai vizsgálatoknak a kielemzése legalább két okból kihívást jelentett a szakembereknek: a gyulladásos faktorok mennyisége és összetétele nagyon gyorsan tud térben és időben változni, és több százat kellett közülük egyszerre tanulmányozni. A gyulladás egy rendkívül komplex reakciója a szervezetnek, amiben az adott fertőzésre nem specifikus fehérjék is részt vesznek, vagyis óriási zajból kell kihalászni a COVID-19-re jellemző gyulladásos mintázatot. Ezt Dénes szerint már nagyon nehéz a hagyományos módszerekkel elvégezni, így kapóra jött, hogy a kutatás során Csikász-Nagy Attila és csoportja az elemzést saját gépi tanulási (machine learning) algoritmusukkal tudta elvégezni. A módszer nemcsak, hogy nagyon hatékonyan tud változásokat kimutatni rengeteg adatban, de olyan mintázatokat is észrevehet, amiket a kutatók nem. „Itt pontosan ez történt” – mondta Dénes, és így végeredményként össze tudtak állítani egy 8 fehérjéből álló csomagot, amik jól és specifikusan mutatják a COVID-19 hatását. A gyulladásos válasz szabályozásában kulcsszerepet játszó fehérjék azonosításában több hazai és nemzetközi partner mellett fontos szerepet vállalt Benkő Szilvia, a Debreceni Egyetem Élettani Intézetében működő kutatócsoportja is.
Ha megvan az a néhány biomarker fehérje, ami erős összefüggést mutat a betegséggel és súlyosságával, akkor Dénes szerint a tudománynak előbb-utóbb sikerül őket biológiai mechanizmussal párosítania. Ezután jöhet a következő lépcsőfok, a gyulladásos folyamatba beavatkozó terápia kifejlesztése, és annak meghatározása, hogy milyen módon gátolhatók hatékonyan a kimutatott gyulladásos faktorok vagy fehérjékből álló hálózatok. „Itt megint csak egy hosszú folyamat elé nézünk” – mondta, hiszen meg kell nézni, hogy mely fehérjék gátlásának van hatása a betegségre egy sejttenyészetben vagy állatmodellben, aminek megvannak a maga kihívásai.
Szerencsére már most is vannak eszközeink arra, hogy a poszt-covid szindróma kialakulásának kockázatát csökkentsük és tüneteit mérsékeljük. Az Európai Járványügyi Központ (ECDC) március végi jelentése szerint a covidoltás 27 százalékkal csökkentheti az elhúzódó tünetek kialakulásának valószínűségét. Eközben pedig Dénes szerint úgy tűnik, hogy a fizikai aktivitás fenntartása – amennyiben ez lehetséges – a kevés olyan megoldás között van, ami segíthet a poszt-covidos betegeken. „A fizikai aktivitásnak az egyik legfőbb ismert hatása az, hogy képes a krónikus gyulladást a szervezetben csökkenteni” – mondta, aminek alapjait szintén érdemes tovább vizsgálni. Bár magát az idegi károsodást nagyon nehéz visszafordítani, számos poszt-covidos betegnél látszik egy lassú állapotjavulás. „Az idegrendszernek van egy regenerációs kapacitása” – mondta a kutató, és ha az elhúzódó gyulladásos folyamatokat gátolni lehetne, akkor ezt még hatékonyabbá lehetne tenni.
Dénes szerint a covidjárvánnyal az orvosok és a neurológusok kézzelfogható bizonyítékot kaptak arra, hogy a szervezetben beinduló gyulladásos folyamatok milyen komoly idegrendszeri tüneteket képesek okozni. Ebből pedig jó esetben az következhet, hogy nagyobb figyelmet és több kutatási forrást kaphatnak az idegrendszeri betegségek hátterében meghúzódó gyulladásos folyamatok megértését célzó vizsgálatok. Ha ennek fontosságát a döntéshozók is belátják, nemcsak a COVID-19-hez hasonló, vagy éppen a krónikus vírusfertőzések neurológiai hatásait érthetjük meg jobban, hanem felkészültebben nézünk majd szembe a jövő járványaival és a gyakori idegrendszeri betegségek hátterének megértésével is.
Kapcsolódó cikkek a Qubiten:
Kapcsolódó cikkek


Mennyire vagyok védett a most terjedő vírusvariánsok ellen, ha már elkaptam az omikront?

Egy titokzatos archea vizsgálatával közelebb jutottunk a komplex élet kialakulásának megértéséhez